消化管は食べることができるものを選ぶ
金沢和樹
神戸大学大学院農学研究科
生命機能科学専攻
食品・栄養科学分野 教授
ヒトの消化管は体内に取り込んで利用できるものとできないものを選別する能力を持っています。そして、機能性成分やサプリメントは体内にほとんど取り込みません。例外的に取り込む成分もあります。これらの詳細を以下で議論してみようと思います。
消化管の選別機能
消化管は、食べた食物成分の中から、体内に取り込んで利用することができる物とできないものを選別します。とくに胃と、体内吸収を主に担っている小腸は、体内吸収してはいけないものを排除する防御器官です。例えば、食品に含まれている脂質が酸敗すると脂質過酸化物が生じます。脂質過酸化物、食品の場合は主に中性脂質(トリアシルグリセロール)のヒドロぺルオキシド(TL-OOH)です。
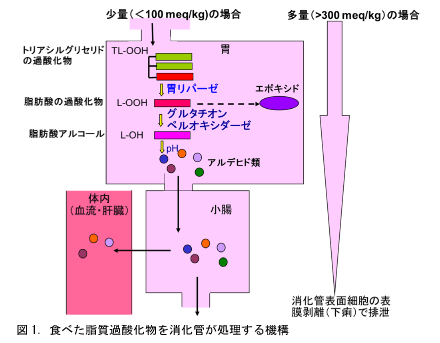
この酸敗食品あるいは酸敗した調理油を食べると、消化管は図1のように、過酸化物を無害な物質に分解して便に捨てます。仮に脂質過酸化物が体内に取り込まれると、体内でヒドロキシラジカルなどの活性酸素を発生させ、体タンパク質や遺伝子などを酸化して傷害をおこします。そこで、胃はTL-OOHを胃リパーゼでグリセロールから外して脂肪酸の過酸化物(L-OOH)とし、次に、グルタチオンペルオキダーゼで脂肪酸アルコール(L-OH)にします。そして、酵素的か非酵素的かは不明ですが、L-OHを低分子のアルデヒドと酸に分解して小腸に移します。小腸の上皮細胞はアルデヒド類をアルデヒド脱水素酵素で酸化して一部を取り込みますが、ほとんどは便に排泄します。これは、過酸化物価(PV)が100 meq/kg以下の脂質過酸化物が少量の場合ですが、食品の基準値は10 meq/kgあるいは30 meq/kg以下で、現代人が多量の過酸化物を食べることはありません。現在の市販食品のPVはもっと低く、最大でも2 meq/kg、通常は0.1 meq/kg以下です。この微量の過酸化物でも、仮に体内に取り込まれれば過酸化連鎖反応を誘発して、体内で多量の過酸化物を産生します。しかし、消化管は私たちが知らないうちに食事過酸化物をすべて無害な形に処理しているのです。かつて、60年ほど前に酸敗したインスタント食品で食中毒事故がおこったことがありましたが、そのときのPVは数百meq/kgでした。仮に、この数百meq/kgの脂質過酸化物を食べたとしても、人の消化管は図1に示すように、小腸の表面細胞が剥離をおこして、すべての過酸化物を下痢で排泄します。正に消化管は、身を挺して、からだを異物や毒物から護っているのです。つまり、消化管は、からだが利用できるものとできないものを選別するのです。
機能性成分も選別される
では、「体内で利用できるもの」とは何かですが、それを定義すると「生命を維持するためのエネルギー源として、また、そのエネルギー代謝で利用できるもの」です。利用しやすいものから順に並べると、糖質、タンパク質、脂質、ビタミンと一部のミネラルです。これらは、体内の酵素が認識してもとの形をとどめないまでに代謝分解(異化)して、化学エネルギーにする、あるいはその代謝酵素に必須の成分です。例えば糖質のグルコースは、炭素6個の化合物が解糖系で3つの化合物になりTCA回路で1つの化合物になります。この過程で水素イオンに変換されます。さらに水素イオンは電子伝達系でATPの化学エネルギーに変換されます。つまり、もともと炭素数6つの明確な化学構造をもっていた物質が、化学エネルギーという形のない形態に変換されるのです。タンパク質や脂質も、からだの構成成分となるというそれぞれの役割が終わると、アミノ基が外されて、解糖系とTCA回路でグルコースと同じように異化されます。そしてその過程で、生命維持に必須のエネルギーを得るのです。これが、生命にとっての「利用」です。
一方、近年話題の機能性成分はどうでしょう。「食品に含まれていたときの化学形態のままで体内に取り込まれるから効く」と考えられているのではないでしょうか。もし、「食べたときの化学形態のままからだに取り込まれれば」、それは生命にとっては大変危険な状況です。体内酵素が認識できない、代謝できない物質が、体内を循環すれば、体内物質に無作為に作用して、生命維持にもっとも大切な「恒常性」を崩します。例えで説明しますと、繊細な実験をしている研究室に、まるで科学など知らないセールスマンが訪れて、実験中の研究者たちに売り込み話をしたとしたら。その結果の混乱を説明する必要はないでしょう。そこで、通常はまずアポを取って、受付で案内を得てから、限られた範囲で研究室を見学します。機能性食品の成分も同様です。
図2にポリフェノールのフラボノール、ケルセチンの一例を示しました。
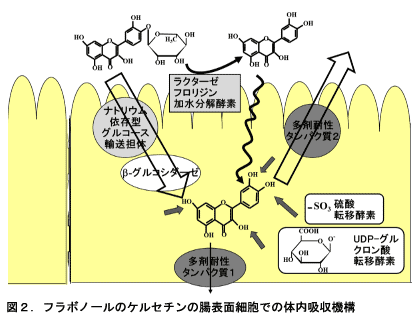
ポリフェノールのほとんどは、腸表面細胞でこのように処理されます。糖を結合した配糖体のポリフェノールは、腸表面細胞のナトリウム依存型グルコース輸送担体で細胞内に取り込まれた後、β-グルコシダーゼで糖とポリフェノール骨格(アグリコンと称する)とに加水分解されます。あるいは腸表面に存在するラクターゼフロリジン加水分解酵素で糖とアグリコンとに加水分解された後に、糖は糖の吸収機構によって、アグリコンは単純拡散で表面細胞内に取り込まれます。いずれにしても、摂取したポリフェノールは腸表面細胞内に一時的にアグリコン形態で存在します。しかし、腸表面細胞はこのアグリコンを速やかに、「取り扱いやすい化学形態」に処理します。ヒトのからだの60%は水ですから、その水に溶けて輸送しやすい化学形態に変換するのです。例えばケルセチンの場合は、水酸基(OH基)が5つありますが、その4つのうちのいずれか1つに水によくなじむ糖のグルクロン酸あるいは硫酸を付けるのです。これを「抱合」といいます(図のケルセチンのキノン基の左隣のOHは水素結合で6員環を形成しますので、この位置は抱合されません)。グルクロン酸や硫酸で抱合されたポリフェノールは水によく溶けて細胞内を動き回ることができますから、すぐに多剤耐性タンパク質2に捕まって、細胞外、つまり管腔側に放出されて便に排泄されます。一部が多剤耐性タンパク質1で体内、つまり血流側に放出されますが、その量はごく微量です。しかも、抱合されていますから生理活性はありません。
機能性成分の生理活性は大きく2つに分けることができます。抗酸化能とタンパク質機能調節作用です。抗酸化能は体内の過剰な活性酸素を消去してからだを酸化ストレスから護る機能です。しかし、還元因子を供給する水酸基が抱合されているのですから、抗酸化能はのちに述べる限られた成分以外は発揮できません。タンパク質機能調節作用とは、酵素、受容体、輸送担体などの体タンパク質の疎水ポケットに作用して、可逆的にそのタンパク質の活性を調節する機能です。しかし、抱合されて親水性に変わっているポリフェノールにこの作用はありません。つまり、体内に取り込まれた機能性成分はその機能をほとんど発揮できないのです。グルクロン酸や硫酸で抱合する抱合酵素の活性はたいへん高く、抱合物を細胞外に排泄する輸送担体の活性も高いので、食べた機能性成分は、抱合酵素や多剤耐性タンパク質が認識できない低濃度(Km値以下の濃度)しか、ヒトの血中には取り込まれません。したがって、いくらたくさん食べても、ごく微量しか食べなくても、食べた量とは関係なく、体内に取り込まれる機能性成分の濃度はごく微量です。
ヒト体内に取り込まれた量を測定したデータが多くあります。Manachの総説に報告されているデータの一部を表1に抜粋してみました。ポリフェノールの体内濃度はマイクロモル以下で、ほとんどがナノモルレベルです。しかも、そのほとんどが生理活性のない抱合体です。筆者が測定した結果では(未発表)、生理活性を発揮できるアグリコンの量は表1の濃度のおおよそ50分の1でした。
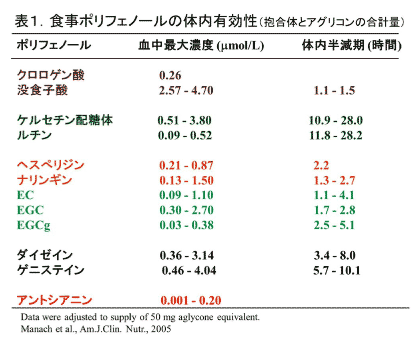
つまり、抱合酵素のKm値の一桁低い濃度が抱合を受けていないアグリコン形態のポリフェノールの体内濃度と思われます。多くの酵素のKm値は10-6Mですが、酵素はその一桁低い10-7M濃度まで基質を認識できて抱合できるので、抱合を逃れた基質、つまりアグリコン形態のポリフェノールの濃度は10-7M、数十nMレベルということになります。
さらに、表の右端のカラムは体内に取り込まれたポリフェノールの体内寿命を示していますが、数時間から1日あまりです。アミノ酸などの栄養素の体内半減期は80日から120日ですから、体内に取り込まれたポリフェノールの寿命がいかに短いかが判ります。ポリフェノールは生命にとってはすぐに排泄すべき必要でない成分であることを意味しています。
体内吸収される成分を探し出すには
「サプリメントに機能性があれば、病気を予防するなどで生命維持に好ましいではないか」というのは人の勝手な主張であって、生命にとってエネルギー化できない食品成分は、たとえそれが長い目でみると健康維持に好ましい作用を示すかもしれなくとも、エネルギーをつくり出し、それを利用することで生き延びている生命にとっては、エネルギー産生を混乱させるかもしれない物質であって、抱合で無害化して排泄しなければならない異物あるいは毒物です。例えば医薬です。病気を治療する、症状を緩和するからといって、生命はその薬を体内に取り込みません。薬を開発する研究者は、その物質が抱合を受けずに生理活性を維持したまま、あるいは脂溶性物質に混ざって単純拡散で有効に体内に取り込まれるようにドラッグデザインをしなければなりません。たいへんな基礎データと知恵と試行錯誤を求められる研究です。さらに、体内に取り込まれたならば、それまでに体内に存在しなかった物質ですから、毒性を発揮する可能性があります。そこで、副作用を厳密に調べなくてはなりません。これに対して機能性食品の場合は、もともと食経験がいくらかある食品の成分ですから、副作用に関してはあるていど緩く考えられ、安全性試験も医薬ほど厳しくありません。
そこで、この「食経験」があるという点を活かして、体内に取り込まれ生理活性を発揮できる成分を探し出すのが、機能性食品開発のポイントです。その探索アイデア8つを、成功具体例を示しながら、以下で論じます。
体内に取り込まれたごく低濃度で機能性を示す成分
食べたポリフェノールの体内濃度は数十nM以下で、ほとんどが抱合されていると説明しました。しかし、その低濃度でも生理活性を示すポリフェノールがあります。
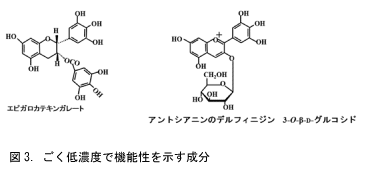
これまでに見出されているのは 図3に示したエピガロカテキンガレートと、一部のアントシアニンです。エピガロカテキンガレートは39.9 nMという低濃度で67-kDaラミニン受容体に作用してがん予防効果などを示すと報告されています。エピガロカテキンガレートは図で判るように、抱合の標的となる水酸基を8つ持っています。多くの水酸基を持つので、その一つが抱合されても物性は大きく変化せず、体内でタンパク質機能調節作用を示すと思われます。アントシアニンはプラスチャージした化学構造ですから、糖が外れると開環して分解します。つまり、配糖体が安定な化学形態です。そして、配糖体はごく微量がナトリウム依存型グルコース輸送担体を介して体内に取り込まれます。また、配糖体は水溶性なのでそれ以上の抱合は受けません。しかし、異化できないフラボノイド骨格をもつ化合物ですから、生体はその排泄場所を探し、もっとも末梢の皮膚あるいは眼の網膜に一時的に排泄します。つまり、皮膚や眼に一時的に局在するのです。アントシアニンの体内濃度は30 nMほどですが、それが局在すると抗酸化能などの生理活性を示します。ベリー類のアントシアニンを食べて、眼の疲れが癒されたと体感する人が多いのはこの局在性によります。一時的に蓄積したアントシアニンは、摂るのを止めると徐々に尿に排泄されて1週間ほどすると消えます。長期間蓄積して副作用を示すことはありません。
このような低濃度で機能性を示す成分は稀です。将来、エピガロカテキンガレートやアントシアニン以外の機能性成分が発見される可能性は低いと思います。
体内吸収時に代謝変換をほとんど受けない成分
これに当てはまる成分は2種類あります。一つは、上であげたアントシアニンのように抱合体と同じように糖などを結合している化合物、また、抱合を受けるべき水酸基やアミノ基が何らかの置換基でマスクされている化合物です。図4にその例をあげました。柑橘に特異的なポリメトキシフラボンのノビレチンは水酸基のすべてがメチル基でマスクされていますので、抱合は受けず、そのままの化学形態で4.6~10 μMという濃度で体内に取り込まれます。そして、様々な機能性が見出されています。また、アルカロイドのカフェインは抱合の標的である窒素にメチル基が付いており、これもこの化学形態のままで体内に取り込まれます。そして、気分を落ち着かせる、眠気を覚ます、皮膚がんを予防するなどの顕著な機能性を体感する人が多く居ます。
あてはまる成分のもう一つがテルペノイド類です。テルペノイドは自然界に約25,000種類ありますが、カロテノイドもテルペノイドの一種です。機能性が注目されているテルペノイドの一部を図5に上げました。テルペノイドは図5のものにかぎらず、その多くが抱合を受けずに体内に取り込まれます。また、その体内吸収もポリフェノールの場合とは異なり、食べた量に比例します。吸収率は0.1%から数%と低いですが、多く食べれば食べた量に比例して多くを体内に取り込みます。例えば、ミカンをたくさん食べると手が黄色くなります。これはミカンに含まれるβ-クリプトキサンチンが末梢の皮膚に一時的に溜まったからです。昆布やワカメに含まれるフコキサンチンを多量にマウスに与えると、体毛も臓器もフコキサンチンの橙色に染まります。しかし、血液の生化学検査や組織学的検査でも、全く異常は検出されません。そして、数週間すると尿に排泄されて橙色は消えます。この一時的な体内蓄積の間に、がん予防やメタボリックシンドローム改善などの顕著な効果を示すと報告されています。
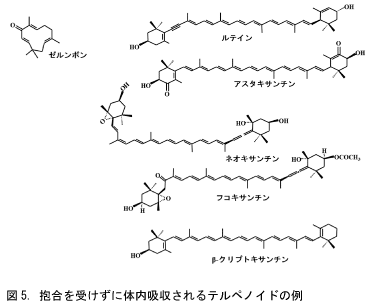
テルペノイドの種類は多いので、将来新たな機能性を示すテルペノイドが発見される可能性は高いと思います。また、柑橘類は特異的にポリメトキシフラボノイドを生産しますので、ノビレチン以外に顕著な機能性を示すフラボノイドが見出される可能性も高いと思います。
抱合酵素が接近しにくい化学構造の成分
食品成分を抱合して便に排泄する抱合酵素は、水酸基やアミノ基などの親水性の官能基に、より親水性が高い糖や硫酸を付加する酵素です。したがって、抱合酵素の活性部位は親水性アミノ酸で構成されています。そこでもし、基質となる化合物の抱合を受けるべき官能基が疎水性基で覆われている場合は、おそらく抱合酵素は接近できず、抱合できないと考えられます。図6に示した化合物がその例です。左端のアルテピリンCはブラジル中部に生育するバッカリス・ドラクリクンフォリアという植物が生産する成分です。この植物から密や樹脂を集めるミツバチはアルテピリンCを多量に含むプロポリスをつくります。このアルテピリンCが抱合を受けるか否かを測定してみると、ごく一部しか抱合を受けず、与えた量の数%が体内に取り込まれました。そして、顕著な大腸がん予防効果を示しました。アルテピリンCの抱合を受ける官能基は水酸基ですが、その両隣に疎水性のプレニル基が付いています。このプレニル基が抱合酵素の接近を妨げたのだろうと考えられます。図6の中央の化合物はカンゾウの成分のグラブリジンです。カンゾウは古代からローマ帝国や中国で親しまれ、その有効性が認められている漢方です。
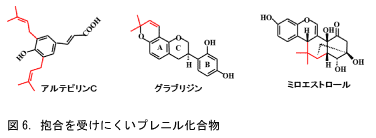
甘味成分のグリチルリチンとともに含量が高いのがこのグラブリジンで、動物試験でもヒト試験でも摂取した数%が抱合を受けずに体内に取り込まれています。そして、腎炎予防、抗炎症、抗酸化能などの機能性が報告されています。A環の水酸基がプレニル基で覆われていますので、これが抱合を妨げていると思われます。また、右端の化合物は南アジアに生育するクズに含まれるミロエストロールです。これも抱合を受けにくく、体内に取り込まれて、きわめて強いエストロジェン様作用を示します。
植物の天敵は植物を食べる昆虫や動物です。植物は食べられることから身を護るために、有害な物質をつくります。昆虫や動物はその有害物質を抱合して無毒化します。植物はそれに対抗して、抱合されにくい化合物をつくり出したと考えられます。プレニル基やプレニルが2つのゲラニル基を持つ植物成分は、この数年間に多様に発見されています。プレニル化合物は植物化学分野での大きな研究課題の一つですから、将来あらたに、顕著な機能性を示すプレニルあるいはゲラニル化合物が見出される可能性は高いと思います。
抱合された後も機能性を残している成分
残している機能性は抗酸化能です。図7はタマネギに豊富なフラボノールのケルセチンが還元因子を放出することで抗酸化能を発揮する機序を示したものです。ケルセチンはA、B、Cの3環からなり5つの水酸基と1つのキノン基を持っています。環を形成している結合と水酸基やキノン基の結合はすべて共役して安定しています。そしてB環の3’と4’の水酸基は還元因子を放出しやすく、放出した後のジキノン構造も共役二重結合で安定しています。
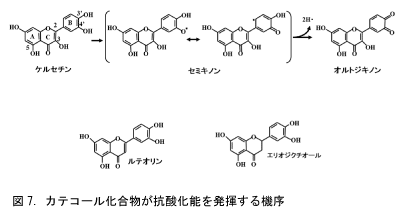
このベンゼン環に水酸基が隣接して2つ付いている化学構造をジオールあるいはカテコールといいますが、カテコール構造の化合物は例外なく顕著な抗酸化能を示します。言い換えれば、生体内に存在するごく微量でも抗酸化能を発揮できるのはカテコール構造の化合物です。そして、カテコール化合物の中でも、ケルセチンはその化学構造のすべての結合が共役二重結合なので、もっとも顕著な抗酸化能を示します。図7の下段に、葉菜に含まれるフラボンのルテオリンとレモンなどの柑橘に含まれるフラバノンのエリオジクチオールの化学構造を示しました。ルテオリンは3位に水酸基がないので、この部分の結合は共役に関与しません。エリオジクチオールは2と3の結合が飽和結合でこの結合は共役二重結合を形成しません。したがって、ルテオリンもエリオジクチオールも他のポリフェノールに比べると強い抗酸化能を示しますが、ケルセチンには劣るわけです。
同様に、コーヒーの主成分のクロロゲン酸、生体成分のドーパミンやアドレナリンは単環のカテコール構造で、強い抗酸化能を示します。しかし、ケルセチンには劣ります。一方、ベンゼン環に水酸基が3つ付いたトリオールならば、還元因子をより多く放出できるので抗酸化能はより強いはずだという主張があります。トリオールの、フラボンのバイカレインやフラボノールのミリセチンなどはたいへん顕著な抗酸化能を発揮します。しかし、還元因子を放出した後の化学構造は、トリキノンです。きわめて不安定な構造で、分解してアルデヒド化合物などを生じます。つまり、抗酸化能を発揮すると壊れてしまい、リサイクルが効かないのです。また、生じたアルデヒドが体タンパク質に結合して毒性を示す場合があると報告されています。例外的に、毒性を示さず、ケルセチンよりも顕著な抗酸化能を発揮するトリオールは、ガロカテキンやカテキンガレートのみです。
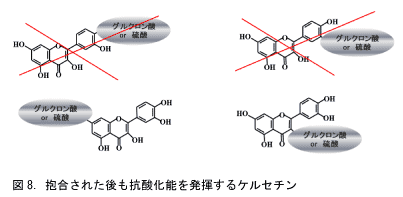
ところで、なぜケルセチンが体内吸収時に抱合されても、体内で抗酸化能を維持しているかですが、図8を見てください。ケルセチンが抱合を受ける水酸基は4つあると上で述べましたが、その4か所を図8に示しました。B環の3’あるいは4’が抱合を受けるとカテコール構造が消えます。一方、3位あるいは7位が抱合を受けても、B環のカテコール構造は維持されています。つまり、3位あるいは7位が抱合されたケルセチンは抗酸化能が発揮できるのです。そして、3’と4’は等価ですから一つと数えることができますので、ケルセチンが抱合後も抗酸化能を維持している確率は3分の2となります。ヒトにケルセチンを摂取させ、その血液中のケルセチンの抗酸化能を測定した研究があります。血中ケルセチンの抗酸化能は、食べたケルセチンに対して約60%であったと報告されています。
代謝変換されて生理活性を示す成分
もともとはほとんど機能性を持たないが、体内吸収時に腸内の微生物や腸表面細胞の酵素によってその化学構造が少しアレンジされることで機能性が現れる食品成分があります。図9はその例です。ウコン(ターメリック)に含まれるクルクミンは、腸細胞の酵素によってヒドロクルクミンに代謝されることが見出されています。クルクミンの生理活性はそれほど高くないのですが、テトラデヒドロクルクミンはきわめて顕著な機能性を示します。それは、直鎖部分が不飽和結合であるクルクミンは左右にベンゼン環がぶら下がったバーベル様ですが、飽和結合になると炭素鎖が折れ曲がりベンゼン環同士が近づきます。その結果、ケトンの酸素が突き出した形になり、その酸素が生体の解毒活性を担っている受容体のNrf2-Keap1に作用しやすくなるからであろうと推測されます。そして、ウコンのサプリメントは肝機能を改善するといわれて好まれています。
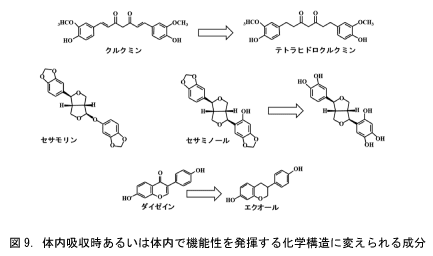
セサモリンやセサミノールはゴマを焙煎してゴマ油を製造するときに生じる物質ですが、いずれも生理活性はほとんどありません。しかし、体内に取り込まれると体内の酵素によってメチル基が加水分解で外され、カテコール構造に変換されます。カテコール構造は上で述べたように強い抗酸化能を示します。そして、これらを用いたサプリメントはヒトでも効果があると報告されています。
エクオールはイソフラボンのダイゼインの腸内細菌による代謝物であることはよく知られています。ダイゼインも弱いエストロゲン様作用を持っていますが、エクオールはより明確なエストロゲン様作用を示し、骨粗鬆症、乳がん、子宮がんなどを予防すると報告されています。
このような体内吸収時に活性化される成分は、探せばまだまだ見いだせると思います。将来の研究が期待されます。
炎症組織のβ-グルクロニダーゼで脱抱合されて活性化する成分
異化することができない、つまり代謝分解してエネルギー源とすることができない物質は、生体にとっては異物、場合によっては毒物だと上で述べました。仮に異化できない物質が体内に存在すると、生体はそれを何らかの方法で処理しなければならないので、生体にとっては大きな負担になります。だから、生体は異化できない物質を抱合によって、体内タンパク質などに作用できない化学形態に変換します。つまり、抱合体は副作用を示さず、生体にとっては安全な物質です。しかし、生体のどこかに異常が生じて病気になりかけたときに、何も機能してくれない物質は、役に立たない不要物です。ところが、興味深い現象があります。発がん物質などの毒物によって炎症がおこりがん化しつつある組織では、β-グルクロニダーゼという抱合を外す脱抱合酵素を漏出しています。この酵素によって、体内を循環していた抱合体は脱抱合されてアグリコンとなり、抗酸化能を発揮する、あるいは炎症細胞をアポトーシスに誘導するなどで、がん予防効果を示します。つまり、細胞ががん化しつつあった当人には自覚のない状態で、この物質はがんを予防したわけです。まさに理想的な医食同源物質ですが、この作用が認められて報告されているのは、今のところ図7のケルセチンとルテオリンだけです。
将来、新たな物質が発見される可能性は高いと思います。それを見出すポイントは、もともと機能性がきわめて顕著な食品成分を探し出すことです。機能性が顕著だから、無作為に体成分に作用されては恒常性が乱れるので、生体はそれを抱合するのです。そして、それが脱抱合されれば、もとの顕著な機能性を、脱抱合酵素が漏出している局所で、発揮します。
抱合されにくいように化学構造が類似の成分を複数組み合わせる
食品成分の機能性を研究する場合、研究者はその有効成分をできるだけ純粋に調製して、動物あるいはヒトに与えます。そして多くの場合、もとの粗雑な混合物だったら効いたのに、純品にしたら効果がなくなってしまった、という結果によく出くわします。これは言うまでもなく、消化管の選別機能です。消化管の表面細胞の抱合酵素活性はきわめて高く、一種類の物質を多量に与えても、それが「異化できない」物質ならば、そのほぼすべてを抱合して排泄します。ところが、私たちは日常の食生活で、食事によって体調が改善した、病気が治ったなどの体験をもっています。食事では多種類の「異化できない」物質を同時に摂ります。例えば、キャベツを食べると、キャベツに含まれているフラボノールのケルセチンとケンフロール、フラボンのルテオリンの3種類を同時に摂ることになります。以下は筆者の研究結果からの推測です。ヒトの腸細胞の抱合酵素は60種類ほどですが、ヒトが食べる「異化できない」物質は数千種類以上ですので、一つの抱合酵素が基質とする物質は「フラボンとフラボノール類」というような、ある程度の広がりをもっているようです。さらに、フラボンとフラボノール類を基質とする抱合酵素は、比較的頻繁に食べる物質のケルセチンに対して基質特異性が高いという特徴がありました。その結果、ケルセチン、ケンフェロール、ルテオリンを同時に摂ると、ケルセチンはほぼすべて抱合されて排泄されるが、ケンフェロールとルテオリンの一部は抱合を受けずに体内に取り込まれるという現象が観察されました。抱合を受けていないアグリコン形態のフラボノイドは強い機能性を発揮します。フラボノイドを複数同時に摂取すると、何らかの機能性が期待できると思われます。
食品成分を組み合わせるというのは、多種多様なアイデアがあり、それを考える人の独創性もありますので、機能性食品の開発にまだまだ大きな余地を残している分野と思われます。
体内吸収されずに腸上皮細胞を介して免疫調節などの機能を示す成分
この成分は、言うまでもなく、最近研究が精力的に行われている食物繊維です。細菌の細胞壁は多糖で覆われています。ヒトの腸表面細胞は、ビフィズス菌や乳酸菌の細胞壁の多糖を、O-157などの菌の細胞壁多糖と区別して認識し、ビフィズス菌や乳酸菌を常在菌とすることで、腸内から細菌をすべて排除するという過応答を避け、Th-1とTh-2の免疫応答バランスを保っている、ということはこの数年に明らかにされたことです。この菌の細胞壁の多糖が、食物繊維です。そして、キノコに豊富な食物繊維のβ-グルカンにも、免疫応答バランスを調節するという機能が認められています。ところで、このβ-グルカンなどの食物繊維は、その一部が体内に加水分解吸収されて体内で機能性を発揮するという説と、体内に取り込まれることはなく、消化管の表面細胞に作用して何らかのシグナルを体内に伝えるという説に分かれています。筆者は後者の説を支持しています。Caco-2細胞とマクロファージとの共培養系にβ-グルカンを与えると、β-グルカンはCaco-2の層を通過することなく、マクロファージからの腫瘍壊死因子分泌を抑えます。これはCaco-2細胞とマクロファージの間に何らかの情報交換があり、その情報を刺激あるいは遮断する物質を、β-グルカンがCaco-2細胞に分泌させているからだと考えられます。また、海藻のマコンブの食物繊維の一つはF-フコイダンですが、F-フコイダンは全く消化吸収されません。にもかかわらず、ヒトの血中のエイコサノイド分泌を調節して血栓症を予防するという明確な作用を示しました。フコイダンにはいくつかの種類があり、F-フコイダンはフコースと硫酸化フコースで構成されています。ワカメのフコイダンはガラクトース(G)を含むG-フコイダンで、モズクはウロン酸(U)を含むU-フコイダンです。G-フコイダンやU-フコイダンは、その一部が消化吸収されて体内に取り込まれるという報告がありますが、F-フコイダンはモノクロナール抗体で測定すると、食べたすべてが糞便から検出されました。体内吸収されない物質の生体に対する作用機序を解明するのは、様々な手法的困難が伴います。しかし、言い換えれば、将来が期待される研究分野だということです。食物繊維の化学構造は、それを生産する生物の種類によって少しずつ異なります。つまり、生物の種類だけ食物繊維は存在します。新規の食物繊維に機能性が見出される可能性は高く、興味深い研究分野です。
(2012年12月)





